El desarrollo embrionario es un proceso extraordinario y complejo, un ballet de células que, partiendo de una única entidad, da lugar a la intrincada arquitectura de un organismo completo. En el contexto de las técnicas de reproducción asistida (RA), la transferencia del embrión a la cavidad uterina se realiza típicamente en la etapa de blastocisto, o en fases previas a su completa formación. Los embriólogos clínicos están familiarizados con las etapas del desarrollo embrionario preimplantacional y las tecnologías emergentes, como la embriocinética, que enriquecen constantemente nuestro conocimiento sobre este fascinante proceso. Sin embargo, simultáneamente a la implantación, cuando el trofoectodermo invade el endometrio, la masa celular interna (MCI) del blastocisto experimenta transformaciones vertiginosas que culminan en la formación del embrión propiamente dicho. Este es un proceso de trascendental importancia conceptual, ya que en esta fase un grupo de células con pluripotencialidad para originar cualquier tipo celular, comienza a establecer los esbozos de los futuros órganos en sus posiciones correctas, y las células se comprometen a sus destinos de forma prácticamente irreversible.
Del Blastocisto al Disco Embrionario: Los Primeros Pasos de la Organización
Aunque las etapas previas a la gastrulación difieren significativamente entre mamíferos y otros vertebrados, principalmente debido a variaciones en el proceso de segmentación influenciado por el tamaño de los gametos femeninos, una vez que se forma el disco embrionario y se inicia la gastrulación, los mecanismos de desarrollo para establecer el futuro organismo siguen patrones notablemente similares en todos los vertebrados. Este fenómeno, conocido como convergencia evolutiva, subraya la relevancia fundamental de la gastrulación. Podemos concebir esta secuencia orquestada de procesos de desarrollo durante la gastrulación como un cuello de botella evolutivo, esencial para la formación de un nuevo organismo en todos los vertebrados. Por esta razón, gran parte de la información crucial sobre la gastrulación se ha obtenido del estudio de organismos más accesibles para la experimentación, como las aves, en comparación con los embriones de mamíferos.
Cuando el blastocisto es transferido, la MCI está compuesta por un número relativamente pequeño de células, alrededor de 50. La proliferación celular incrementa rápidamente este número, sin una reducción apreciable en el volumen celular, una característica distintiva de las divisiones previas durante la segmentación. Simultáneamente a este aumento celular, la MCI deja de ser una estructura desorganizada. A través de procesos complejos y aún no completamente dilucidados, se organiza en una masa ligeramente aplanada o discoidal, conocida como el disco embrionario.
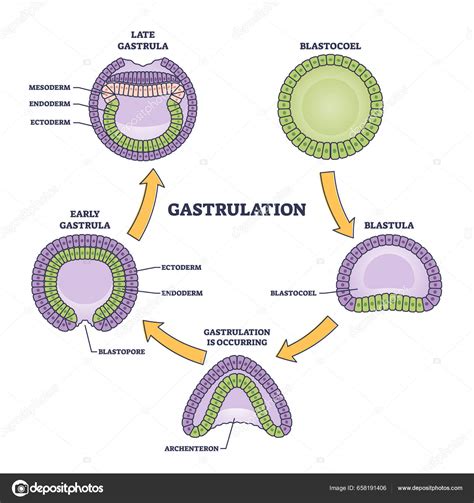
La Gastrulación: Un Viaje Migratorio para Establecer las Capas Germinales
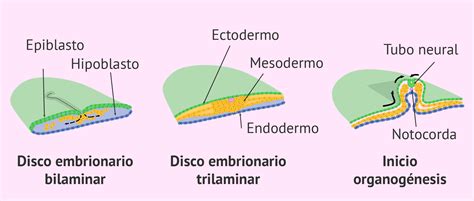
En las fases tempranas del desarrollo, las células del ectoblasto (epiblasto) inician dos procesos fundamentales y concomitantes: la división celular para aumentar su número y la migración para ocupar nuevas posiciones en el embrión. Numerosas células del epiblasto se dirigen hacia el hipoblasto, desplazando sus células y dando lugar a la formación de una nueva capa celular: el endodermo.
El inicio de la gastrulación se caracteriza por cambios morfogenéticos significativos. Las células del ectodermo se dividen y migran para formar la tercera capa germinal: el mesodermo. Estas células ectodérmicas, con una alta capacidad de proliferación, siguen corrientes migratorias celulares en dos direcciones principales: una corriente látero-medial y otra rostro-caudal.
La línea primitiva es la estructura morfológica que emerge cuando las células ingresan a través de ella para formar el mesodermo. Las células que siguen la migración rostro-caudal se invaginan en la región más rostral de la línea primitiva, formando progresivamente una estructura alargada y central a lo largo de la capa media del embrión. Esta estructura, conocida como la notocorda o mesodermo axial, se extiende por el eje embrionario longitudinal. Un análisis detallado de la migración celular a través de la línea primitiva revela un sector claramente definido y de diferente significación funcional en su extremo rostral. En esta posición, donde las células del ectodermo rostral se invaginan para dar lugar a la notocorda, se encuentra una zona embrionaria primordial denominada el organizador, o nódulo de Hensen, nombrado en honor a su descubridor.
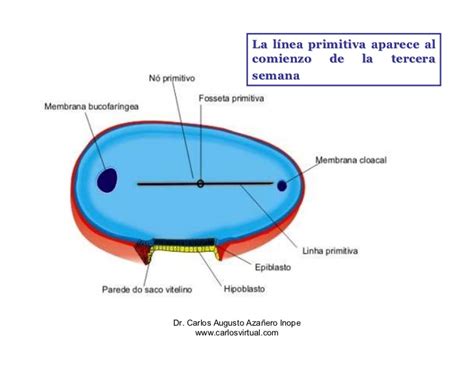
Es importante destacar que la notocorda, formada por la migración rostro-caudal de células del epiblasto a través del nódulo de Hensen, no se configura completamente entre las capas ectodérmica y endodérmica en las regiones más craneales del embrión. En estas áreas, una íntima unión entre el ectodermo y el endodermo impide la penetración de las células de la notocorda.
La gastrulación es un proceso dinámico que determina el desarrollo progresivo en estas fases iniciales. Dado que las células de las regiones rostrales inician la división y migración antes que las de las regiones caudales, el desarrollo embrionario sigue una secuencia rostro-caudal. Un embrión en desarrollo mostrará sus tres capas germinales (ecto-, meso- y endodermo) ya establecidas en su sector rostral (craneal o cefálico), mientras que el sector caudal aún estará en proceso de formación de la línea primitiva.
La Divergencia y Convergencia de las Capas Germinales: Hacia la Formación Tridimensional
A partir de esta etapa, el embrión comienza a crecer y a adquirir progresivamente su forma tridimensional. Este desarrollo se produce a través de dos vías fundamentales: la diferenciación de cada una de las tres capas para formar órganos y aparatos específicos, y la incurvación del cuerpo embrionario en sentido céfalo-caudal y lateral para configurar su estructura tridimensional.
Aunque el desarrollo de cada capa da lugar a distintos órganos, aparatos y sistemas, es crucial comprender que el desarrollo de cada una es coincidente y concomitante con el de las otras dos. Las tres capas se desarrollan simultáneamente. Además, durante el proceso morfogenético de cada capa, existen interacciones tisulares, celulares y moleculares significativas entre sus componentes y entre las capas mismas, de modo que los procesos en una capa repercuten en el desarrollo de las demás.
El ectodermo constituye la capa más externa y superficial del embrión. Forma parte de las paredes que delimitan el espacio que rodea al embrión, el saco amniótico.
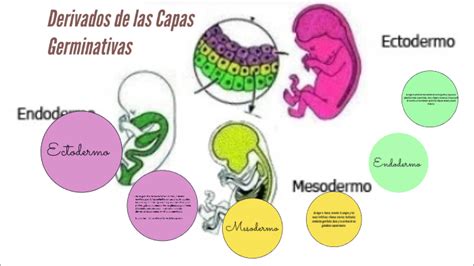
Si bien todas las estructuras del mesodermo se desarrollan simultáneamente, es pertinente analizar primero el componente mesodérmico situado en el eje longitudinal del embrión: la notocorda. Originada por la migración rostro-caudal de las células epiblásticas más craneales, la notocorda se extiende a lo largo de todo el embrión, excepto en la zona más rostral, donde la placa precordal interfiere. La notocorda desempeña un papel fundamental en la inducción neural de la capa ectodérmica suprayacente. Así, el ectodermo neural es la región ectodérmica longitudinal en íntima relación con la notocorda. Experimentos clásicos en embriones de pollo han demostrado que la extirpación de la notocorda resulta en la ausencia de diferenciación del ectodermo neural, y viceversa, la implantación experimental de una segunda notocorda induce la diferenciación de dos regiones ectodérmicas neurales.
El mesodermo para-axial se caracteriza por su división progresiva en sentido céfalo-caudal, dando lugar a pares de acúmulos celulares situados a cada lado de la notocorda, formando los somites. El número de pares de somites es un indicador del avance del desarrollo embrionario y se utiliza como criterio para determinar la edad del embrión. Los somites sufren diferenciación celular, dando lugar a tres líneas: el dermotomo (que formará la dermis), el esclerotomo (que formará estructuras cartilaginosas y óseas como costillas y vértebras) y el miotomo (que formará las estructuras musculares).
El mesodermo lateral se divide rápidamente en dos hojas: la hoja somatopleura (en relación con el ectodermo) y la hoja esplacnopleura (en relación con el endodermo). Estas hojas se fusionan con las del lado opuesto a nivel de la línea media a medida que el embrión se pliega, formando el cuerpo embrionario. El mesodermo es un claro ejemplo de la especificación del destino celular durante la gastrulación.
El endodermo es la capa embrionaria más profunda, en íntima relación con el saco vitelino. Aunque muestra los cambios morfogenéticos menos evidentes inicialmente, participa activamente en el desarrollo. Sigue el proceso de incurvación embrionaria, dando lugar a la formación del tubo endodérmico que recorre el embrión longitudinalmente desde la boca primitiva (estomodeo) hasta el ano (membrana cloacal).
GASTRULACIÓN | Desarrollo embrionario | Ectodermo Mesodermo y Endodermo
Neurulación y la Aparición del Sistema Nervioso: Un Proceso Temprano y Crucial
Si bien todas las estructuras germinales se desarrollan de manera simultánea, algunos órganos y aparatos muestran indicios de diferenciación antes que otros. Uno de los cambios morfogenéticos más precoces es la diferenciación del ectodermo neural, que marca el inicio del desarrollo del sistema nervioso alrededor de la tercera semana de gestación. Este proceso, denominado neurulación, abarca la formación de la placa neural, los pliegues neurales y su cierre para formar el tubo neural, completándose aproximadamente hacia la cuarta semana de desarrollo.
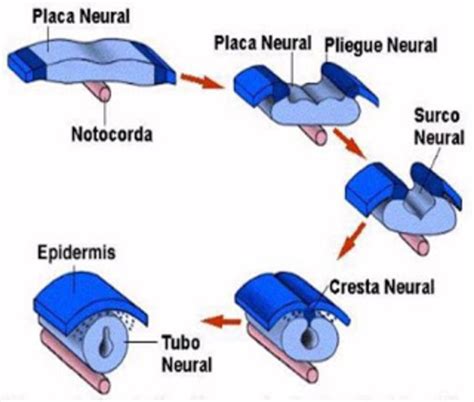
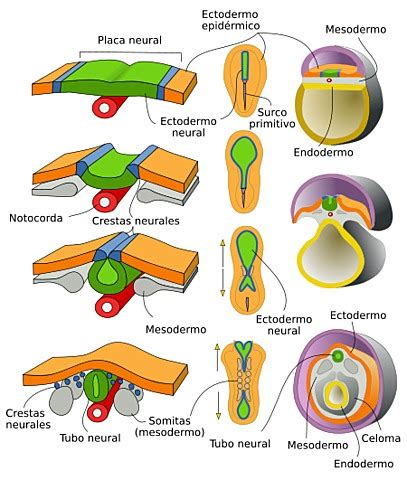
La placa neural se forma por un engrosamiento del ectodermo, inicialmente relacionado con el nódulo de Hensen y posteriormente con el mesodermo axial (la notocorda), extendiéndose en sentido cráneo-caudal. La placa neural se invagina longitudinalmente, formando el canal neural y el surco neural, flanqueado por los pliegues neurales. Estos pliegues se aproximan y cierran progresivamente, constituyendo el tubo neural.
El tubo neural dará origen al sistema nervioso central: el encéfalo y la médula espinal. La luz del tubo neural, el conducto neural, formará las cavidades ventriculares y el conducto ependimario. Al finalizar el cierre del neuroporo rostral, el segmento más craneal del tubo neural da lugar al desarrollo del encéfalo, inicialmente caracterizado por la formación de las tres vesículas cerebrales primarias: prosencéfalo, mesencéfalo y rombencéfalo. La pared del tubo neural está compuesta por neuroepitelio cilíndrico pseudoestratificado, que evoluciona a medida que la estructura histológica se configura.
El sistema circulatorio es la primera unidad funcional en constituirse, con el corazón funcionando desde aproximadamente la tercera semana para suplir las necesidades nutricionales y de oxígeno del embrión, que ya no pueden satisfacerse por difusión a medida que este se vuelve más complejo.
Los Discos Imaginales: Arquitectos del Cuerpo de los Insectos
En el reino de los invertebrados, particularmente en insectos holometábolos como la mosca Drosophila melanogaster, el desarrollo de los órganos adultos se lleva a cabo a partir de estructuras llamadas discos imaginales. Estos son sacos epiteliales que crecen en el interior de la larva y que, durante la metamorfosis, se desarrollan para formar órganos específicos en el insecto adulto, como ojos, antenas, alas y patas.
Cada disco imaginal está programado para dar lugar a un conjunto determinado de estructuras. Por ejemplo, la mayoría de los órganos de la cabeza, como los ojos, las antenas, la cápsula cefálica y los palpos, derivan de un único tipo de disco. La producción de señales de comunicación intercelular y de factores de transcripción, que regulan la expresión génica en grupos celulares específicos y en momentos determinados, es esencial para la diferenciación, el crecimiento y la organización de los tejidos. Estos procesos están orquestados por redes genéticas que operan durante el desarrollo de los discos imaginales.
En Drosophila melanogaster, se ha observado que los discos imaginales no se corresponden directamente con metámeros (segmentos corporales), sino con porciones anteriores o posteriores de estos. La investigación ha demostrado la especificidad y la función intrínseca de los discos imaginales, evidenciando que las células que los componen están especificadas tempranamente en la embriogénesis. Un disco imaginal, como el del ala, puede contener decenas de miles de células, mientras que discos más pequeños, como los de la pata, albergan alrededor de diez mil.
A diferencia de la mayoría de las células larvarias con capacidad mitótica limitada, los discos imaginales proliferan rápidamente en momentos específicos. A medida que las células se multiplican, forman un epitelio tubular que se pliega sobre sí mismo en una espiral compacta. Durante su desarrollo, las células se restringen a regiones de destino específico. Al final de la etapa larval, justo antes de la pupación, el disco es un saco epitelial conectado por un delgado tallo a la epidermis de la larva, un tallo que juega un papel crucial en la posterior eversión del disco.
Durante la última etapa larval y la primera etapa pupal, el disco alcanza su tamaño final, su morfología comienza a cambiar y se diferencia en su estructura adulta. Al inicio de la pupación, las células del centro del disco se extienden hacia afuera para formar las porciones más distales de la estructura, mientras que las células externas dan lugar a las estructuras proximales. Tras la diferenciación, las células de los apéndices y de la epidermis secretan una cutícula específica para cada región.
Aunque el disco está compuesto principalmente por células epidérmicas, un pequeño número de células adepiteliales migran hacia el disco en etapas tempranas del desarrollo. La especificación de los destinos celulares generales ocurre en el embrión. En Drosophila melanogaster, existen nueve pares de discos imaginales y un disco impar.
La generación del tipo de estructura de la pata, por ejemplo, está determinada por las interacciones entre varios genes dentro del disco imaginal. El centro del disco secreta altas concentraciones de los morfógenos Wingless (Wg) y Decapentaplegic (Dpp) durante el tercer estadio larval. Estas altas concentraciones provocan la expresión del gen Distal-less, que dirige la formación de las estructuras más distales de la pata, como las garras y los segmentos tarsales. Concentraciones moderadas de Dpp inducen la expresión del gen dachshund, mientras que concentraciones más bajas activan el gen homothorax. La expresión de dachshund conduce a la formación del fémur y la tibia proximal, y las áreas de superposición entre homothorax y dachshund dan lugar al trocánter y la tibia distal.
La diferenciación del disco también requiere una señal hormonal, una serie de pulsos de la hormona 20-hidroxiecdisona (20E). Los ejes del ala se especifican mediante patrones de expresión génica que dividen al embrión en compartimientos interactuantes. La expresión del gen engrailed distingue el compartimiento posterior del ala del anterior. El factor de transcripción Engrailed activa el gen hedgehog en el compartimiento posterior. Hedgehog, a su vez, actúa como un factor de transcripción de corto alcance para activar la expresión del gen decapentaplegic (Dpp) en una estrecha banda de células en la región anterior del disco del ala. Dpp actúa como un factor paracrino difusible de largo alcance, estableciendo un gradiente de concentración que activa genes como spalt y oculomotor blind (omb) en altas concentraciones, y solo omb en bajas concentraciones. El eje dorsoventral del ala se forma mediante la expresión del gen apterous en las células dorsales prospectivas. En el límite entre los compartimientos dorsal y ventral, los factores de transcripción Apterous y Vestigial interactúan para activar el gen wingless.
Los discos de ojo y antena son particulares porque producen diferentes estructuras adultas. Estas regiones se subdividen en primordios que darán origen a antenas, ojos compuestos y regiones específicas de la cápsula cefálica. El surco morfogenético, que atraviesa el epitelio del disco, comienza en el tercer estadio larval y diferencia las células de la retina. Dpp, Wg y hh están involucrados en la regulación del progreso del surco. Mutaciones sugieren que la expresión de hh en la diferenciación de células fotorreceptoras induce la expresión de Dpp en células anteriores adyacentes y la progresión del surco. La expresión temprana de Dpp a lo largo de los márgenes posterior y lateral del disco es necesaria para la iniciación del surco. Además de su rol en la formación del surco, Dpp previene el destino de cabeza en el primordio del ojo, mediante la represión de Wg y el gen homeótico orthodenticle (odt). La represión de Wg por Dpp permite el desarrollo del ojo compuesto. hh también es necesario para la progresión del surco morfogenético y la diferenciación de los omatidios, y juega un papel temprano en el patrón global del disco de ojo-antena, ya que en su ausencia, Dpp no se expresa en el disco posterior del ojo.
Eventos de transdeterminación, donde un disco imaginal adquiere un destino diferente al programado originalmente, pueden ser inducidos por la no-expresión de proteínas homeodominio y la proteína nuclear Vestigial. Cuando el daño a los discos imaginales es difuso, intercalando células muertas con células sobrevivientes, la proliferación de estas últimas se incrementa, un fenómeno conocido como proliferación compensatoria.
Los Discos Intervertebrales: Estructuras de Soporte y Absorción de Impacto
En contraste con los discos imaginales de los insectos, el término "disco" en anatomía humana se refiere a los discos intervertebrales. Estas son estructuras fibrocartilaginosas situadas entre las superficies adyacentes de las vértebras. La columna vertebral humana contiene 23 discos intervertebrales: 6 en la región cervical, 12 en la torácica y 5 en la lumbar. Cada disco consta de un anillo fibroso externo que rodea un núcleo central gelatinoso, el núcleo pulposo.
El desarrollo del disco intervertebral se inicia en la quinta semana de gestación. Las células mesenquimales de los esclerotomas, que rodean la notocorda, migran cranealmente para formar el disco intervertebral. A medida que el desarrollo progresa, la notocorda degenera y desaparece al ser rodeada por los cuerpos vertebrales en desarrollo. Sin embargo, entre las vértebras, la notocorda se expande para formar el núcleo pulposo. Posteriormente, este núcleo se rodea de fibras dispuestas circularmente, formando el anillo fibroso, compuesto por 15-25 anillos concéntricos o laminillas de fibras de colágeno paralelas, orientadas alternativamente a 60 grados con respecto al eje vertical. El núcleo pulposo contiene fibras de colágeno organizadas aleatoriamente y fibras de elastina dispuestas radialmente. La placa terminal, una capa delgada de aproximadamente 1 mm de espesor, se interpone entre el disco y el cuerpo vertebral.
Una característica notable de los discos intervertebrales, al igual que otros cartílagos, es su falta de irrigación sanguínea propia, lo que los convierte en las estructuras más grandes del cuerpo desprovistas de vasos sanguíneos. Durante el desarrollo embrionario y al nacer, poseen una vascularización limitada que alcanza sus placas terminales y el anillo fibroso, pero estos vasos sanguíneos desaparecen rápidamente, dejándolos avasculares en la vida postnatal y adulta. Los discos intervertebrales están inervados por los ramos meníngeos de los nervios espinales.
Las anomalías de los discos intervertebrales pueden manifestarse como dolor de espalda, dolor de cuello y ciática. Otras causas de estos síntomas incluyen estenosis espinal, artrosis de columna y espondilolistesis. Una hernia discal, o hernia del núcleo pulposo, ocurre cuando el material gelatinoso del núcleo pulposo escapa de los confines del anillo fibroso, pudiendo ejercer presión sobre un nervio espinal cercano.
Antes de los 40 años, aproximadamente el 25% de las personas muestra evidencia de degeneración discal. El envejecimiento y la degeneración discal provocan la deshidratación del núcleo pulposo y una disminución en la concentración de proteoglucanos, lo que reduce su capacidad de absorción de impactos. Esta reducción general del tamaño del disco contribuye a la disminución de la altura observada con la edad. El anillo fibroso también se debilita con el tiempo, aumentando el riesgo de desgarros.
Las Microvellosidades: Amplificando la Superficie para la Absorción y Señalización
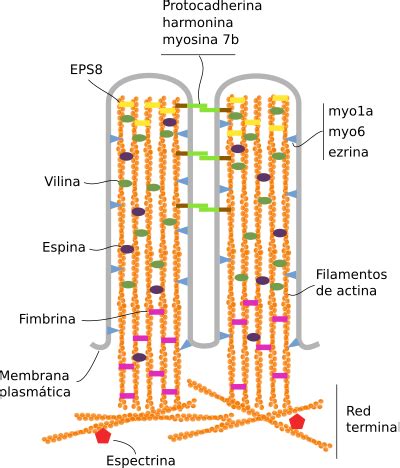
En el ámbito celular, las microvellosidades son prolongaciones citoplasmáticas delgadas que se extienden desde la membrana plasmática de células diferenciadas, especialmente aquellas con superficies libres como las células epiteliales. Estas estructuras filiformes, de 1 a 2 µm de altura y unos 100 nm de grosor, contienen en su interior decenas de filamentos de actina dispuestos paralelamente a su eje principal. Generalmente, las microvellosidades se encuentran densamente empaquetadas, formando lo que se conoce como un ribete en cepillo.
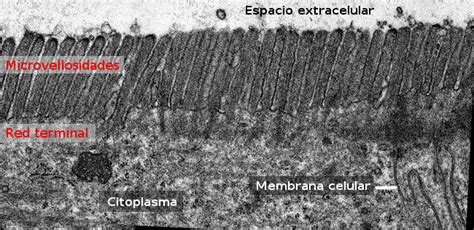
Las microvellosidades se forman mediante la asociación de filamentos de actina a una placa densa en la superficie interna de la membrana plasmática. Proteínas como la vilina y la fimbrina son cruciales para agrupar y estabilizar estos filamentos de actina, mientras que la ezrina ayuda a conectar el haz de filamentos a la membrana. La elongación y organización de las microvellosidades, incluyendo la formación de conexiones laterales mediadas por protocadherinas, ocurren en fases posteriores. La actividad exocítica es necesaria para aportar los componentes de membrana y proteínas de superficie necesarios para la evaginación de la membrana plasmática impulsada por la polimerización de actina.
La estructura de las microvellosidades se mantiene gracias a un entramado de 30 a 40 filamentos de actina internos, unidos por fimbrina y vilina, y conectados a la membrana celular por Myo1A y calmodulina. El esqueleto de actina se extiende hacia el citoplasma, entrelazándose con microfilamentos de otras microvellosidades para formar una red terminal en el citoplasma cortical apical. A pesar de su estabilidad aparente, el citoesqueleto de las microvellosidades sufre una renovación continua, con una renovación completa estimada cada 20 minutos. Alteraciones en la concentración de calcio o el inicio de la división celular pueden inducir la desaparición de las microvellosidades.
La principal función de las microvellosidades es maximizar la superficie de la membrana plasmática para el intercambio de sustancias entre los tejidos y el medio extracelular. Esto es particularmente importante en células absortivas o secretoras, como las del epitelio digestivo y los túbulos renales, donde pueden aumentar la superficie hasta 100 veces. Las microvellosidades albergan proteínas transportadoras, canales iónicos y receptores, facilitando la absorción de nutrientes y la secreción de sustancias.
Además de su papel en el transporte, las microvellosidades regulan la transducción de señales. Su estructura permite una interpretación relativamente independiente de la información molecular del resto de la célula, funcionando como antenas. El denso empaquetamiento de las microvellosidades también actúa como una barrera física protectora, por ejemplo, contra parásitos en el epitelio digestivo.
Ciertas microvellosidades especializadas, como los estereocilios, desempeñan funciones sensoriales. Estas estructuras modificadas, presentes en el epidídimo y en las células sensoriales del oído interno, son mecanorreceptores que captan movimientos de fluidos. Los fotorreceptores, especialmente en invertebrados, pueden derivar su membrana fotosensible de microvellosidades, formando estructuras llamadas rabdómeros que contienen pigmentos fotosensibles.
Las microvellosidades también participan en la generación de vesículas extracelulares, liberando pequeñas vesículas desde la superficie de los enterocitos mediante la acción de su citoesqueleto.