El glucógeno, un polisacárido complejo, representa la principal forma de almacenamiento de energía en los animales. Su estructura, caracterizada por cadenas ramificadas de glucosa, le confiere una notable solubilidad en agua, permitiendo la formación de dispersiones coloidales. Esta particularidad estructural, similar a la amilopectina del almidón pero significativamente más ramificada, es fundamental para su función biológica, facilitando la rápida liberación de glucosa cuando el organismo así lo requiere. El glucógeno se acumula de manera estratégica en dos órganos vitales: el hígado, donde constituye aproximadamente el 10% de su masa, y los músculos, representando alrededor del 1% de su masa muscular en los vertebrados.
Biosíntesis del Glucógeno: Un Proceso Energéticamente Demandante
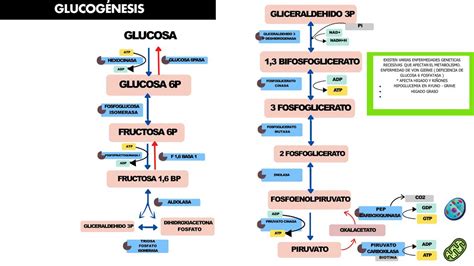
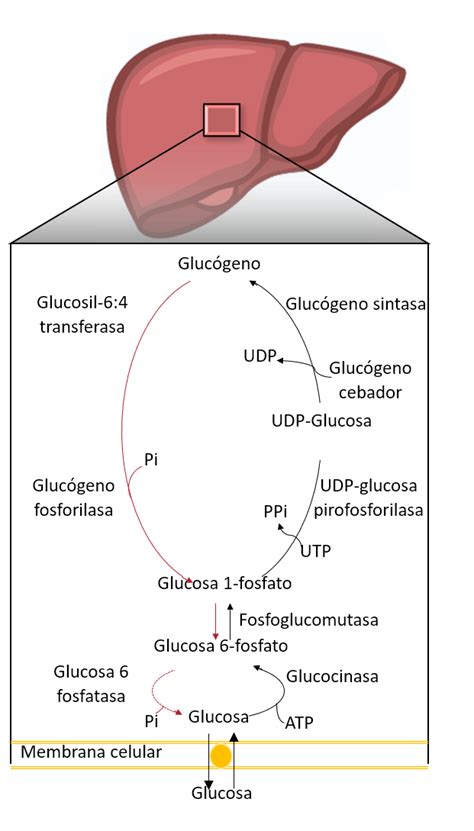
La formación de glucógeno a partir de glucosa, conocida como glucogénesis, es un proceso anabólico que requiere energía. Inicia con la entrada de glucosa a las células, donde es fosforilada a glucosa-6-fosfato. Esta reacción es catalizada por la hexocinasa o, en el hígado, por la glucocinasa. Posteriormente, la enzima fosfoglucomutasa reorganiza la glucosa-6-fosfato a glucosa-1-fosfato. Para que la glucosa-1-fosfato pueda ser incorporada a la cadena de glucógeno en crecimiento, debe ser "activada" metabólicamente. Este paso crucial implica la reacción de la glucosa-1-fosfato con trifosfato de uridina (UTP) para formar uridina difosfato-glucosa (UDP-glucosa) y liberar pirofosfato inorgánico. La UDP-glucosa es, por lo tanto, la forma metabólicamente activa de la glucosa para la síntesis de glucógeno.
La enzima clave en la síntesis de glucógeno es la glucógeno sintasa. Esta enzima es la principal responsable de la regulación de todo el proceso. La glucógeno sintasa transfiere unidades de glucosa desde la UDP-glucosa a los extremos no reductores de una cadena de glucógeno preexistente. Es importante destacar que la glucógeno sintasa solo puede añadir glucosa a cadenas que ya contengan al menos cuatro residuos de glucosa, lo que significa que se requiere un "cebador" o molécula inicial para iniciar la síntesis.
La Importancia de la Ramificación en la Estructura del Glucógeno
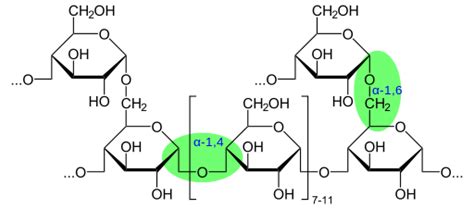
La estructura altamente ramificada del glucógeno es una de sus características más distintivas y funcionales. La síntesis de glucógeno no solo implica la polimerización lineal de unidades de glucosa mediante enlaces α-(1→4), sino también la creación de puntos de ramificación mediante enlaces α-(1→6). En este proceso interviene una enzima especializada conocida como enzima ramificante o amilo-(1,4 → 1,6)-transglucosilasa.
Esta enzima actúa transfiriendo segmentos de glucosa, típicamente de unos 11 o más residuos, desde el extremo no reductor de una cadena lineal en crecimiento a una cadena vecina. Al hacer esto, crea un nuevo punto de ramificación con un enlace α-(1→6). La ramificación es crucial porque genera múltiples extremos no reductores a los que la glucógeno sintasa puede unirse, acelerando significativamente la velocidad de síntesis y, de manera recíproca, la velocidad de degradación cuando se necesita glucosa. Cada punto de ramificación duplica efectivamente la cantidad de sitios disponibles para la adición de glucosa, lo que permite un almacenamiento y una movilización de energía mucho más eficientes. La enzima desramificante del glucógeno juega un papel crucial en la degradación, pero la enzima ramificante es indispensable para construir la estructura tridimensional del glucógeno.
Degradación del Glucógeno: Liberando Energía para la Acción
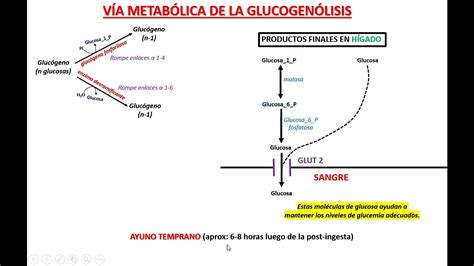
La degradación del glucógeno, conocida como glucogenólisis, es el proceso mediante el cual se liberan unidades de glucosa para ser utilizadas por el organismo. Este proceso es especialmente vital para mantener los niveles de glucosa en sangre, particularmente durante los períodos de ayuno o cuando la demanda de energía aumenta, como durante el ejercicio físico.
En el hígado, la glucogenólisis está finamente regulada por hormonas como el glucagón y la adrenalina. Cuando los niveles de glucosa en sangre disminuyen, el glucagón es liberado, señalizando al hígado para que descomponga el glucógeno almacenado. La glucosa-6-fosfato liberada de la degradación del glucógeno hepático es desfosforilada por la enzima glucosa-6-fosfatasa y luego liberada a la circulación sanguínea para ser utilizada por otros tejidos.
En los músculos, la glucogenólisis tiene un propósito autolimitado. El glucógeno muscular sirve como una fuente de energía de rápida disponibilidad para las contracciones musculares. A diferencia del hígado, el músculo carece de la enzima glucosa-6-fosfatasa. Por lo tanto, la glucosa-6-fosfato generada a partir de la degradación del glucógeno muscular se canaliza directamente hacia la glucólisis dentro de la propia célula muscular, sin ser liberada a la sangre.
La enzima principal en la degradación del glucógeno es la glucógeno fosforilasa. Esta enzima escinde secuencialmente las unidades de glucosa de las cadenas de glucógeno mediante la adición de un grupo fosfato inorgánico (fosforólisis), rompiendo los enlaces α-(1→4) y liberando glucosa-1-fosfato. Sin embargo, la glucógeno fosforilasa no puede actuar sobre los enlaces α-(1→6) que se encuentran en los puntos de ramificación. Para eliminar estas ramificaciones y permitir que la fosforilasa continúe su acción, se requiere la acción de una enzima desramificante del glucógeno. Esta enzima tiene una actividad transferasa que mueve una cadena corta de glucosa desde la rama a la cadena principal, y una actividad hidrolítica que rompe el enlace α-(1→6), liberando glucosa libre.
El Papel del UDP en el Metabolismo del Glucógeno y Más Allá
La uridina difosfato (UDP) es una molécula de nucleótido esencial que desempeña un papel central en múltiples procesos metabólicos y de síntesis en las células. Su importancia en el contexto del metabolismo del glucógeno radica en su participación en la formación de UDP-glucosa, la forma activada de glucosa necesaria para la glucogénesis. La UDP-glucosa pirofosforilasa cataliza la reacción entre la glucosa-1-fosfato y el UTP para formar UDP-glucosa, liberando pirofosfato inorgánico.
Más allá de la síntesis de glucógeno, la UDP es un precursor vital en la síntesis de otros nucleótidos, como el trifosfato de uridina (UTP) y el difosfato de citidina (CDP). También es fundamental en la glucuronidación, un proceso de desintoxicación donde la UDP-glucuroniltransferasa (UGT) utiliza UDP-glucurónico para conjugar moléculas con ácido glucurónico, facilitando su excreción. Además, la UDP es un intermediario clave en la síntesis de otros polisacáridos importantes, como los glicosaminoglicanos, componentes esenciales de la matriz extracelular.
Regulación Hormonal y la Sincronización del Metabolismo del Glucógeno
El metabolismo del glucógeno, tanto su síntesis como su degradación, está intrincadamente regulado por señales hormonales y estados energéticos del organismo. El hígado y el músculo esquelético, aunque ambos almacenan glucógeno, tienen roles ligeramente diferentes. El glucógeno hepático es crucial para mantener la homeostasis de la glucosa sanguínea. Hormonas como el glucagón y la adrenalina, liberadas en respuesta a niveles bajos de glucosa, estimulan la glucogenólisis hepática. En contraste, la insulina, liberada cuando los niveles de glucosa son altos (por ejemplo, después de una comida), promueve la glucogénesis, incentivando el almacenamiento de glucosa como glucógeno.
El glucógeno muscular, por su parte, es una reserva de energía para el propio músculo. Aunque la glucogenólisis muscular también puede ser estimulada por la adrenalina, su principal función es proporcionar combustible para la contracción muscular. La regulación de la glucógeno sintasa es un punto clave. Esta enzima es activa en su forma desfosforilada e inactiva cuando está fosforilada, lo que permite una rápida adaptación a las demandas energéticas.
Regulación de la gluconeogénesis [Hormonal y alostérica]
Implicaciones Clínicas: Cuando el Metabolismo del Glucógeno Falla
Las anomalías en el metabolismo del glucógeno pueden tener consecuencias clínicas significativas. La diabetes mellitus es un ejemplo paradigmático, donde las alteraciones en la producción o acción de la insulina pueden llevar a una acumulación o agotamiento anómalo del glucógeno hepático. En casos de hipoglucemia, provocada por un exceso de insulina, los niveles de glucógeno en el hígado pueden ser elevados, y la insulina circulante puede inhibir la glucogenólisis necesaria para normalizar los niveles de azúcar en sangre.
Además, existen un grupo de enfermedades hereditarias conocidas como glucogenosis, causadas por deficiencias en las enzimas específicas necesarias para la síntesis o degradación del glucógeno. Estas deficiencias pueden manifestarse de diversas maneras, afectando el hígado, los músculos o ambos, y resultando en hipoglucemia, debilidad muscular, o acumulación anormal de glucógeno. Un ejemplo es la enfermedad de Von Gierke, una glucogenosis tipo I, donde la deficiencia de glucosa-6-fosfatasa en el hígado impide la liberación de glucosa libre a la sangre, resultando en hipoglucemia severa y hepatomegalia.
El Glucógeno y el Rendimiento Deportivo: La Estrategia de la Carga de Carbohidratos
Para los atletas, especialmente aquellos involucrados en deportes de resistencia, la gestión de las reservas de glucógeno es fundamental para optimizar el rendimiento. El agotamiento de glucógeno durante el ejercicio prolongado puede llevar a una fatiga extrema, a menudo denominada "golpear el muro" o "la pared del corredor". Para mitigar esto, los atletas emplean estrategias como la "carga de carbohidratos".
Este proceso implica aumentar la ingesta de carbohidratos en los días previos a una competición para maximizar el almacenamiento de glucógeno en los músculos y el hígado. El cuerpo puede adaptar su capacidad de almacenamiento de glucógeno, un proceso conocido como carga de carbohidratos, para satisfacer las demandas energéticas elevadas. Los ciclistas profesionales, por ejemplo, a menudo experimentan el agotamiento del glucógeno en carreras de varias horas, lo que subraya la importancia de mantener estas reservas. La ingesta continua de carbohidratos con un alto índice glucémico durante el ejercicio también ayuda a reponer las reservas de glucógeno y a retrasar la fatiga.
La investigación sobre el glucógeno no se limita a su función energética, sino que también explora su potencial como material de construcción para biomateriales avanzados, destacando la versatilidad y la importancia continua de este polisacárido en la ciencia moderna.
La historia del descubrimiento del glucógeno es fascinante y nos lleva al trabajo pionero del médico y fisiólogo francés Claude Bernard. A mediados del siglo XIX, Bernard fue uno de los primeros en intuir la función glucogénica del hígado. En 1856, su investigación marcó un hito, desafiando las concepciones predominantes sobre la nutrición. En esa época, se creía que solo las plantas podían producir azúcares, que luego eran metabolizados por los animales en un lugar no especificado, que Antoine Lavoisier había hipotetizado que podría ser el pulmón. Bernard, buscando precisamente ese sitio de degradación, observó la presencia de azúcar en la sangre que salía del hígado (vena hepática) y su ausencia en la sangre que entraba (vena porta). Incluso en animales alimentados exclusivamente con carne, la concentración de azúcar en la sangre hepática se mantenía. Sin embargo, debido a las limitaciones de sus métodos de ensayo, que no detectaban concentraciones de azúcar por debajo de 0.8-1 g/L, Bernard no pudo detectar azúcar en la vena porta, lo que lo llevó a una interpretación algo exagerada de sus hallazgos. A pesar de ello, su trabajo sentó las bases para la comprensión moderna del metabolismo del glucógeno.
La síntesis de glucógeno, o glucogénesis, es un proceso complejo que involucra la acción coordinada de varias enzimas. La glucosa que ingresa a las células, ya sea en el hígado o en el músculo, es rápidamente fosforilada a glucosa-6-fosfato. Luego, la fosfoglucomutasa cataliza la isomerización de la glucosa-6-fosfato a glucosa-1-fosfato. El siguiente paso crítico es la activación de la glucosa para su incorporación en el polímero de glucógeno. Esto se logra mediante la reacción de la glucosa-1-fosfato con trifosfato de uridina (UTP) para formar uridina difosfato-glucosa (UDP-glucosa) y liberar pirofosfato inorgánico. Esta reacción es catalizada por la enzima UDP-glucosa pirofosforilasa. La UDP-glucosa es la molécula donante de glucosa para la elongación de la cadena de glucógeno.
La enzima clave en la regulación de la síntesis de glucógeno es la glucógeno sintasa. Esta enzima es responsable de transferir las unidades de glucosa desde la UDP-glucosa a los extremos no reductores de las cadenas de glucógeno preexistentes, formando enlaces α-(1→4). Es importante recalcar que la glucógeno sintasa requiere de una cadena de glucógeno de al menos cuatro residuos de glucosa para iniciar la elongación, actuando sobre un cebador preexistente. La síntesis de glucógeno es un proceso altamente regulado y, en el caso de la glucógeno sintasa, su actividad se controla principalmente a través de la modificación covalente. La enzima es más activa en su forma desfosforilada y menos activa o inactiva cuando está fosforilada.
La estructura ramificada del glucógeno, esencial para su función, se establece mediante la acción de la enzima ramificante, también conocida como amilo-(1,4 → 1,6)-transglucosilasa. Esta enzima toma segmentos de glucosa de una cadena lineal en crecimiento y los une a otra cadena mediante un enlace α-(1→6), creando un nuevo punto de ramificación. Esta ramificación es crucial porque aumenta el número de extremos no reductores disponibles para la acción de la glucógeno sintasa, acelerando así la tasa de síntesis de glucógeno.
La degradación del glucógeno, o glucogenólisis, libera glucosa para satisfacer las necesidades energéticas del organismo. La glucógeno fosforilasa es la enzima principal que rompe los enlaces α-(1→4) del glucógeno, liberando glucosa-1-fosfato. Sin embargo, esta enzima no puede actuar sobre los enlaces α-(1→6) de las ramificaciones. Para ello, se requiere la acción de una enzima desramificante del glucógeno. Esta enzima posee dos actividades: una actividad transferasa que mueve un trisacárido de una rama a la cadena principal, y una actividad hidrolítica que libera glucosa libre al romper el enlace α-(1→6).
El metabolismo del glucógeno está intrínsecamente ligado a la vía de la glucólisis, que es la vía metabólica principal para la obtención de energía a partir de la glucosa. La glucosa-6-fosfato, producto de la degradación del glucógeno, puede ingresar a la glucólisis. En el hígado, la glucosa-6-fosfatasa permite la desfosforilación de la glucosa-6-fosfato, liberando glucosa libre a la sangre para mantener la normoglucemia, especialmente durante el ayuno. En el músculo, la ausencia de esta enzima asegura que la glucosa-6-fosfato se utilice exclusivamente dentro de la célula muscular.
Otras vías metabólicas que interactúan con el metabolismo del glucógeno incluyen la vía de las pentosas-fosfato, que genera NADPH y precursores para la síntesis de nucleótidos, y la síntesis de proteoglicanos y glicoproteínas, que utilizan derivados de la glucosa activada. La regulación hormonal es fundamental. El glucagón y la adrenalina activan la degradación del glucógeno y, al mismo tiempo, inhiben su síntesis. La insulina, por el contrario, promueve la síntesis de glucógeno y suprime su degradación.
El descubrimiento de Claude Bernard sobre la función glucogénica del hígado en 1856 fue un avance monumental. Antes de su trabajo, se creía que los animales dependían exclusivamente de los azúcares de origen vegetal. Bernard observó que el hígado producía glucosa incluso en animales que solo consumían carne, desafiando esta idea. Su meticulosa investigación, a pesar de las limitaciones tecnológicas de la época, lo llevó a identificar la presencia de una sustancia en el hígado que podía ser transformada en glucosa, a la que posteriormente se le dio el nombre de glucógeno. Este descubrimiento sentó las bases para la comprensión de cómo los animales almacenan y movilizan sus propias reservas de energía.
La síntesis de glucógeno, conocida como glucogénesis, es un proceso anabólico que ocurre principalmente en el hígado y los músculos. Inicia con la fosforilación de la glucosa a glucosa-6-fosfato, seguida por la isomerización a glucosa-1-fosfato. La glucosa-1-fosfato reacciona con UTP para formar UDP-glucosa, la forma activada de glucosa que se incorporará al polímero de glucógeno. La enzima glucógeno sintasa es la encargada de añadir las unidades de glucosa a una cadena preexistente, formando enlaces α-(1→4). Para que la estructura sea ramificada, la enzima ramificante transfiere segmentos de glucosa a otras cadenas, formando enlaces α-(1→6). Esta estructura ramificada es crucial para una movilización rápida de glucosa.
La degradación del glucógeno, o glucogenólisis, es el proceso inverso. La glucógeno fosforilasa rompe los enlaces α-(1→4), liberando glucosa-1-fosfato, que luego se convierte en glucosa-6-fosfato. La glucosa-6-fosfato puede entrar en la glucólisis para obtener energía. En el hígado, la glucosa-6-fosfatasa elimina el grupo fosfato, liberando glucosa libre a la sangre. En los músculos, la glucosa-6-fosfato se utiliza directamente en la glucólisis. La enzima desramificante del glucógeno es necesaria para eliminar las ramificaciones y permitir la acción completa de la glucógeno fosforilasa.
La regulación de estas vías es compleja y está influenciada por hormonas y el estado energético celular. El glucagón y la adrenalina promueven la glucogenólisis, mientras que la insulina favorece la glucogénesis. Las deficiencias en las enzimas involucradas en estas vías pueden dar lugar a enfermedades metabólicas, como las glucogenosis. La diabetes, una enfermedad caracterizada por niveles anormales de insulina y glucosa en sangre, también afecta significativamente el metabolismo del glucógeno.
El glucógeno es más que un simple almacén de energía; es un componente dinámico y esencial del metabolismo animal, cuya regulación precisa asegura la disponibilidad de glucosa para diversas funciones fisiológicas. Su descubrimiento por Claude Bernard marcó el inicio de una comprensión más profunda de la bioquímica de los animales y de la homeostasis energética. La intrincada red de reacciones enzimáticas y la regulación hormonal aseguran que este polisacárido cumpla su vital función de reserva energética.